После этого звонка я сделала беглый поиск по базам научных публикаций и нашла лишь несколько статей, посвященных теме, о которой с таким воодушевлением рассказывала Джилл. Для сравнения: РНК-интерференция, изучение которой началось всего-то восемь лет, упоминалась в тот момент уже более чем в четырех тысячах источников (внимание к этой теме достигло апогея, когда позднее в том же году открыватели РНК-интерференции Эндрю Файер и Крейг Мелло получили Нобелевскую премию). Из-за нехватки публикаций было трудно оценить важность темы, о которой говорила Джилл, – но именно это подстегнуло мое любопытство.
Я пробежалась глазами по нескольким обзорным статьям и прочла ровно столько, чтобы понять: эта штука – CRISPR – обозначает участок бактериальной ДНК, а сокращение расшифровывается как “кластерные короткие палиндромные повторы, разделенные регулярными промежутками,
Поиск информации о Джиллиан в
Частично из-за того, что меня так впечатлили исследованияя Джилл, частично из моих собственных научных интересов я все больше хотела с ней встретиться. За четыре года до этого я перешла из Йельского университета в Беркли и переехала в Калифорнию вместе с Джейми Кейтом, который теперь стал моим мужем, и нашим новорожденным сыном Эндрю. Хотя мои текущие исследования уже развивались в некоторых новых направлениях, я надеялась расширить лабораторию и запустить в ней несколько дополнительных проектов, одновременно наладив рабочие связи с новыми коллегами. Возможно, сотрудничество с Джилл – это именно то, чего я ищу.
Мы с Джилл встретились на следующей неделе в кафе
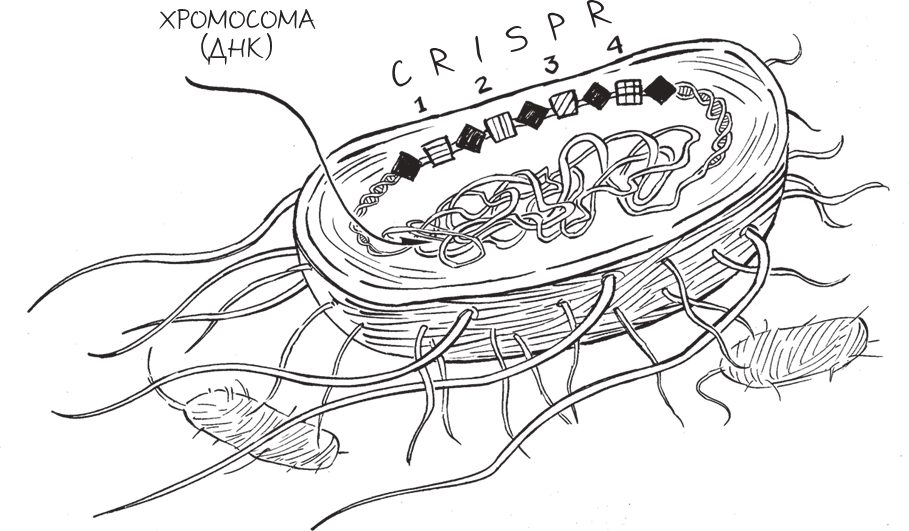
Она быстро набросала схему CRISPR. Сначала изобразила большой овал, он обозначал бактериальную клетку. Затем внутри овала нарисовала круг – бактериальную хромосому, а на одной из его сторон – чередующиеся квадратики и ромбики, символизирующие конкретный участок ДНК. Этот участок, очевидно, и представлял собой CRISPR.
Джилл заштриховала ромбики и объяснила, что все они представляют собой одинаковые последовательности примерно из тридцати “букв” ДНК. Затем она последовательно пронумеровала квадратики, начиная с цифры 1, и сказала, что каждый из них включает в себя уникальную последовательность ДНК.
Наконец я начала понимать слова, скрывавшиеся за аббревиатурой CRISPR
Сама идея, что клетки могут нести в себе повторяющиеся последовательности ДНК, не нова: более 50 процентов генома человека – существенно больше миллиарда “букв” ДНК – это различные типы повторяющихся последовательностей, и некоторые из них представлены миллионами копий. Хотя геномы бактерий сравнительно небольшие, они тоже содержат повторяющиеся последовательности. Я знала о нескольких типах, в названии которых даже присутствовали некоторые слова из расшифровки CRISPR: повторяющиеся экстрагенные палиндромы (
Желая узнать больше об этих странных участках бактериальной ДНК, я спросила Джилл, каковы их биологические функции, но, к моему разочарованию, Джилл ответила, что ничего об этом не знает. Однако в ее лаборатории обнаружили важную зацепку[45]. Последовательности ДНК бактерий природных популяций показали, что буквально каждая клетка в них содержит уникальный вариант CRISPR, поскольку разделяющие регулярные повторы промежутки у каждой клетки отличаются. Это было совершенно необычно, поскольку все остальные участки ДНК у этих клеток практически совпадали. Джилл поняла, что CRISPR, скорее всего, эволюционируют быстрее всех остальных областей генома, а это указывает на то, что их функция – быстро меняться или адаптироваться в ответ на некий вызов из внешней среды, с которым сталкиваются клетки.
Годами ранее испанский профессор Франсиско Мохика в своей новаторской работе[46] обнаружил те же повторы у множества совершенно не родственных друг другу видов, включая архей – одноклеточных организмов, которые, как и бактерии, не имеют ядер. (Бактерии, археи – их собирательное название “прокариоты” – и эукариоты представляют собой три домена, включающих все формы жизни на Земле.) CRISPR, по словам Джилл, обнаружили в половине бактериальных геномов, секвенированных на тот момент, и почти во всех геномах архей. Выходило, что кластерные палиндромы – наиболее распространенный тип повторяющихся последовательностей ДНК у всех прокариот.
Эти факты заставили меня буквально задрожать от любопытства: если CRISPR присутствует у такого большого количества видов, то с высокой вероятностью природа использует этот инструмент для чего-то важного.
Я внимательно слушала, а тем временем Джилл вытащила из стопки бумаг три статьи, все 2005 года[47], и оживленно пересказала их суть. Три коллектива исследователей (один из них – под руководством Мохики) независимо друг от друга обнаружили, что многие спейсеры CRISPR – те фрагменты ДНК, что встроены между повторяющимися последовательностями, – точно совпадают с ДНК известных бактериофагов. Что еще интереснее, возникало ощущение, что между числом последовательностей ДНК в бактериальной CRISPR, совпадающей с вирусной ДНК, и числом вирусов, способных поразить эту бактерию, существует обратная зависимость: чем больше совпадений, тем ниже вероятность инфицирования. Собственное новаторское исследование Джилл[48], в котором геномы целых микробных сообществ были восстановлены секвенированием небольших, перекрывающих друг друга фрагментов ДНК и их сборкой в одну более длинную последовательность, также показало, что многие разделенные регулярными промежутками последовательности на содержащем CRISPR участке хромосомы соответствовали последовательностям вирусной ДНК, обнаруженным в окружающей бактериальные сообщества среде.
В совокупности эти новые сведения стали отличной подсказкой для ответа на вопрос, какую роль CRISPR играет у бактерий и архей. Авторы упомянутых статей обнаружили свидетельство в пользу того, что CRISPR, вероятно, является частью иммунной системы прокариот – адаптацией, позволяющей микроорганизмам успешно справляться с вирусами.
Напоследок, в качестве последнего козыря, Джилл выложила на стол самую новую статью о CRISPR. Опубликованная коллективом исследователей из Национальных институтов здравоохранения под руководством Киры Макаровой и Евгения Кунина[49], она называлась “Гипотетическая иммунная система прокариот, основанная на РНК-интерференции” (
Джилл не смогла бы найти лучшей приманки, чтобы завлечь меня в свои исследования. Не только вся моя научная деятельность до того момента была посвящена изучению молекул РНК, но я еще все больше концентрировалась на процессах РНК-интерференции в человеческих клетках. А тут еще Макарова и Кунин предполагали, что CRISPR представляет собой бактериальный аналог РНК-интерференции. Если это было верно, то моя лаборатория отлично подходит для того, чтобы разобраться с этим новым загадочным биологическим явлением. А перспективы были более чем соблазнительными, поскольку никто еще не провел экспериментов для подтверждения или опровержения теорий о биологическом смысле CRISPR – все только и делали, что плодили эти теории. Для биохимиков, таких как я, это был идеальный момент, чтобы ввязаться в борьбу за понимание того, как работает и для чего нужен CRISPR.
В завершение встречи с Джилл я поблагодарила ее и пообещала быть на связи. Мне нужно было переварить всю новую информацию и просчитать плюсы и минусы добавления исследований CRISPR к текущим проектам моей лаборатории. Если я соглашаюсь заниматься этой темой, мне понадобится ученый, постоянно занятый координацией работы по ней, так как у меня самой не хватило бы времени возглавить новый проект: я была слишком занята руководством лабораторией в целом.
Мне также нужно было освежить свои знания о мире бактерий и о вирусах, которые поражают эти бактерии. Я опубликовала немало научных статей о вирусе гепатита
Фредерик Туорт, британский бактериолог, работавший в начале XX века, стал первым ученым, отметившим действие бактериальных вирусов. По иронии судьбы, изначально Туорт собирался исследовать не вирусы бактерий, а вирусы, поражающие животных и растения, – а они были открыты уже давно. Однако в ходе попыток извлечь вирусы из таких субстратов, как навоз и сено, а затем культивировать их, Туорт обнаружил странную колонию бактерий из рода