Виргиниюс Шикшнис и его коллеги осенью 2012-го опубликовали статью, сходную с нашей[79]; она описывала функции белка Cas9, найденного в производящих йогурт бактериях, относящихся все к тому же роду стрептококков. Как и мы, литовские исследователи обнаружили, что Cas9 разрезает последовательности ДНК, “буквы” которых подходят к “буквам” РНК CRISPR. Но команда Шикшниса не смогла раскрыть важнейшую роль второй РНК (так называемой трансактивационной РНК,
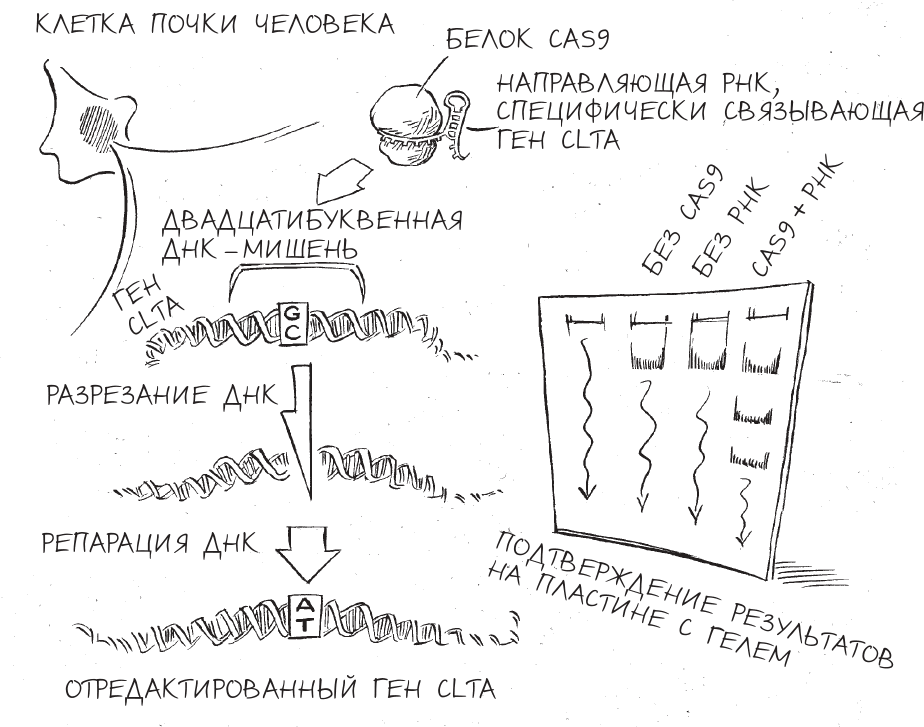
В своей статье мы максимально подробно описали молекулярные требования этой защитной системы и показали, насколько легко и просто можно настроить новые версии CRISPR для разрезания ДНК любым нужным образом. Мы сделали еще один шаг вперед и из направляющей РНК, состоящей у бактерий из двух отдельных молекул РНК (РНК CRISPR и трансактивационной РНК), сделали одну молекулу РНК-гида, тоже дающую Cas9 возможность находить и вырезать определенную последовательность ДНК. Мы также предположили, что эту систему защиты можно настроить на выполнение других функций в клетках – например, не на разрушение вирусной ДНК, а на прицельное редактирование ДНК самой клетки. Если мы поменяем двадцатибуквенный код РНК таким образом, чтобы он был комплементарен последовательности отдельно взятого человеческого гена, и затем введем Cas9 и новую направляющую РНК в клетки человека, CRISPR сделает хирургически точный разрез в гене-мишени, отметив это место как нуждающееся в репарации. Разрезав ДНК, CRISPR приведет клетку в полную боевую готовность, и она устранит внутри себя повреждения – но так, что мы сможем контролировать этот процесс.
Как мы предполагали, использование CRISPR в человеческих клетках подтвердит широту возможностей этого нового способа редактирования генов. И для этих предположений были веские причины. Наше собственное исследование показало, что белок Cas9 и его направляющая РНК очень избирательны и крепко связаны друг с другом, а это свидетельствует, что они без проблем найдут друг друга в человеческой клетке. А что касается отправки их в клеточное ядро, где расположена ДНК, то тут нам достаточно присвоить этим молекулам подходящий химический “адрес получателя”, и клетка сама сделает остальную работу за нас. До этого сотрудники многих лабораторий преуспели в переносе белков и молекул РНК от бактерий в клетки человека, и в нашем распоряжении было немало молекулярно-биологических инструментов, которые помогли бы CRISPR работать должным образом и за пределами его обычных мест обитания.
Нам оставалось только показать, что все работает именно так, как мы и предположили.
Мартин начал с переноса бактериальной ДНК, кодирующей Cas9, и синтезированной на основе информации от CRISPR РНК в две плазмиды – небольшие колечки ДНК, которые ведут себя как искусственные мини-хромосомы. Первая плазмида содержала генетические инструкции для направляющей РНК, а также отдельные инструкции для человеческих клеток, чтобы они тоже понемногу производили такие молекулы РНК. Во второй плазмиде находился ген
Соединив все эти молекулярные компоненты в единую систему, мы с Мартином намеревались превратить человеческие клетки в фабрики для производства CRISPR, которые, сами того не ведая, штампуют молекулы, запрограммированные на разрезание заданных частей собственного генома. И еще мы знали, что CRISPR не убьет человеческие клетки “шинкованием” ДНК, как он делает это с вирусами в бактериях, разрезая вирусную ДНК. ДНК человека (да и всех эукариотических организмов, если уж на то пошло) постоянно получает повреждения – например, это происходит, когда она подвергается воздействию канцерогенных веществ, ультрафиолета либо рентгеновского излучения. И чтобы приводить в порядок поврежденную ДНК, клетки разработали хитроумные системы репарации двуцепочечных разрывов в ней. Таким образом, в самом вероятном сценарии, если CRISPR вырежет нужный ген, клетка ответит на это просто “склеиванием” фрагментов молекулы ДНК обратно в единое целое, будто приварит одну металлическую трубу к другой. Ученые именуют этот процесс негомологичным соединением концов, ведь он, в отличие от гомологичного, не требует ДНК-шаблонов для починки молекулы. (Слово “гомологичный” происходит от греческого
Ключевая особенность этого процесса репарации – заложенная в самой его природе небрежность. Как сварщик перед работой должен удостовериться, что у обеих труб очищены торцы, подлежащие сварке, так и клетке перед соединением фрагментов разорванной ДНК тоже нужно убедиться, что концы этих фрагментов чистые. Создание чистых концов иногда требует удаления или вставки нескольких “букв” ДНК, что приводит к изменениям состава генов после окончания процесса репарации. Это означает, что ген, скорее всего, изменится после “атаки” и вырезания его CRISPR и последующей починки за счет клетки. Этот неточный и порождающий ошибки способ репарации должен был обеспечить нам с Мартином простой метод выявления успешных попыток редактирования генов. Выбирая в качестве мишени конкретный ген и анализируя последовательность его нуклеотидов буква за буквой до воздействия CRISPR и после него, мы могли бы найти любой признак неаккуратной репарации, а это доказало бы, что CRISPR обнаружил свою цель и разрезал ее.
Мы с Мартином решили запрограммировать CRISPR таким образом, чтобы он атаковал человеческий ген, который называется ген легкой цепи клатрина A (
Экспериментальной площадкой для нашего первого испытания редактирования генома должны были стать клетки линии
Эксперименты Мартина тут же продемонстрировали, что мини-хромосомы действительно давали клеткам человеческой почки возможность производить компоненты CRISPR. Когда Мартин изучал эти клетки под микроскопом, он увидел, что значительная доля клеток светилась зеленым, что могло получиться только в результате образования Cas9, связанного с зеленым флуоресцентным белком. Собрав часть клеток и превратив их в кашицу для анализа различных содержащихся в них молекул РНК, Мартин также обнаружил, что клетки почки производили солидные количества направляющей РНК.
Перенос CRISPR из бактериальных клеток в человеческие сработал так, как мы ожидали, но оставался один резонный вопрос: редактирует ли CRISPR ДНК человека?
Мартин и Александра Ист-Селетски, молодая студентка, недавно присоединившаяся к проекту, измельчили еще некоторое количество клеток, выделили из них ДНК и проанализировали состав гена
Всего в несколько простых и хорошо отработанных стадий мы с Мартином выбрали произвольную последовательность ДНК в состоящем из 3,2 миллиарда “букв” геноме человека, спроектировали вариант CRISPR для ее редактирования и стали наблюдать, как крохотная машинерия выполняла то, на что была запрограммирована, – и не где-нибудь, а в живых человеческих клетках. Своими результатами мы подтвердили работу новой технологии, дающей ученым удивительную способность переписать код жизни с хирургической точностью и поразительной простотой. В мгновение ока CRISPR по своему развитию догнал технологии редактирования генома, исследование и разработка которых шли почти двадцать лет.
Фактически в такой же спешке, как и шестью месяцами ранее, когда мы готовили публикацию с Кшиштофом и Эммануэль, мы написали текст научной статьи с изложением наших новейших результатов. Если наша первая публикация 2012 года содержала прямое указание на то, что CRISPR следует применить в качестве новой платформы редактирования генома в клетках, то во второй статье уже содержались четкие демонстрация и подтверждение внушительных возможностей этой недавно открытой системы.
Когда 2012-й подходил к концу, я ощущала заметную иронию, читая, что журнал
К моему глубокому удовлетворению, первые две недели 2013 года ознаменовались публикацией еще пяти научных статей о CRISPR (не считая нашей)[82], и все они описывали сходные эксперименты, в которых эту систему применяли для редактирования генов непосредственно в клетках – как мы и предсказали в 2012-м. И профессор МТИ Фэн Чжан, и гарвардский профессор Джордж Чёрч предварительно связывались со мной, чтобы сообщить о готовящихся публикациях. Статьи Чжана и Чёрча появились на сайте журнала
Это было бурное время. Меня окрыляло то, что наша с Эммануэль работа, опубликованная предыдущим летом, вдохновила других ученых на проведение серий экспериментов, подобных нашим. Лишь позднéе содержание этих статей и даты их публикации начали скрупулезно разбирать и сопоставлять для обоснования той или иной позиции в патентных спорах о CRISPR – досадный поворот событий в истории, которая начиналась как сотрудничество исследовательских коллективов, в атмосфере неподдельного общего восторга по поводу того, что смогут дать человечеству наши исследования!
Сравнив все шесть статей, я осознала, что суммарно в этих экспериментах было отредактировано больше дюжины разных генов. Еще больше радовало разнообразие типов клеток, подвергшихся редактированию. Вдобавок к редактированию генома клеток эмбриональной человеческой почки механизм CRISPR был запрограммирован на то, чтобы разрезать ДНК в клетках человека, пораженных лейкемией, стволовых клетках человека, клетках нейробластомы мыши, бактериальных клетках и даже одноклеточных эмбрионах данио-рерио, популярного модельного организма для генетических исследований. CRISPR не просто демонстрировал отдельные признаки успешного применения; он показывал невероятную гибкость в использовании. Казалось, что любой ген можно сделать мишенью CRISPR, разрезать его и отредактировать, если в клетке присутствует белок Cas9, а направляющая РНК имеет участок, комплементарный двадцатибуквенному коду ДНК.
Ажиотаж вокруг CRISPR усилился в мае, когда лаборатория Рудольфа Йениша в МТИ сообщила о создании мышей с геномом, отредактированным с помощью CRISPR[83]. Всего шестью годами ранее Нобелевскую премию по физиологии или медицине присудили нескольким ученым за разработку методов внедрения изменений в геном мышей – наиболее популярных модельных животных в изучении генетики млекопитающих. Более двадцати лет этот эффективный, но трудоемкий метод был наилучшим – и фактически единственным – способом воспроизведения в организмах мышей мутаций, вызывающих рак или другие болезни у человека. В 1974-м Йениш стал первым, кто создал трансгенную мышь, чьи клетки содержали чужеродный генетический материал, а пятнадцатью годами спустя он вновь вызвал сенсацию, одним из первых применив этот метод, удостоенный Нобелевской премии. А сейчас успех Йениша с CRISPR привлек внимание к новой технологии, которая не просто вытеснила старый подход, но и давала возможность без сучка и задоринки редактировать геномы других животных.